Winkelwagen
U heeft geen artikelen in uw winkelwagen
Monitoring van direct optredende klachten/symptomen tijdens de vaccinatiesessies heeft plaatsgevonden in 2009 en 2010 met behulp van een vragenlijst die tijdens de vaccinatiesessies is verspreid. Hieruit bleek dat directe klachten/symptomen tijdens de vaccinatiesessies vaker optraden tijdens de catch-up campagne in 2009 dan tijdens de reguliere campagne in 2010 (27,1 versus 7,7 per 10.000 doses). (16,18) De meest gerapporteerde direct optredende klacht was (bijna) flauwvallen, dit werd 688 keer gerapporteerd in 2009 (16,8 per 100.000 doses) en 97 keer in 2010 (5,8 per 100.000 doses).
Tijdens de catch-up campagne en tijdens de reguliere campagnes van 2010 en 2014 namen in totaal 4248, 4501 (42%) en 566 (9%) meisjes deel aan vragenlijstonderzoek naar het optreden van klachten/symptomen in de week na de vaccinatie.
Van deze meisjes rapporteerde meer dan 90% een reactie in de week na de 3 opeenvolgende doses (figuur 1) (16-18). In 2014 was de tolerabiliteit van de eerste dosis gunstiger dan van de eerste dosis in 2009 en 2010. Voor de tweede dosis was de tolerabiliteit vergelijkbaar in alle jaren. (13)
Pijn rond de prikplaats en verminderd gebruik van de arm waren de meest gerapporteerde lokale reacties (respectievelijk 70-84% en 48-72%), waarvan 10-30% werd geclassificeerd als ‘veel’. Zwelling en roodheid werden gerapporteerd door 10-20% en 8-15% van de meisjes. Spierpijn was de meest gerapporteerde systemische reactie (55-75%). Ook werden moeheid en hoofdpijn regelmatig gerapporteerd (respectievelijk 19-34% en 18-30%). (16-18)
Er werden geen ernstige of onverwachte klachten/symptomen gerapporteerd. Ten tijde van de derde dosis in 2010 en voor beide doses in 2014 is een aanvullende vragenlijst onder de deelneemsters afgenomen waarin gevraagd is naar het voorkomen van klachten/symptomen in de week vóór de vaccinatie (n≈350 per ronde). Hieruit bleek dat systemische symptomen zoals hoofdpijn en moeheid even vaak of soms zelfs vaker voorkwamen in de week vóór de vaccinatie dan in de week erna (hoofdpijn 28-36% versus 17-26%, moeheid 20-43% versus 18-29%).
In ons land kwamen er tot nu toe bijna 39.000 meldingen van vermoedelijke bijwerkingen na coronavaccinatie binnen bij het FAGG. "Dat is het meest recente cijfer tot en met 3 februari", laat woordvoerder Ann Eeckhout weten. In vergelijking met andere geneesmiddelen ligt dat aantal hier hoger, maar daar is een verklaring voor.
CHECK - Neen, er zijn geen tienduizenden doden in Europa gemeld na coronavaccin
"In vergelijking met andere geneesmiddelen is er veel meer aandacht geweest, nog altijd, voor de coronavaccins", legt Ann Eeckhout uit. "We hebben ook enkele keren opgeroepen om mogelijke bijwerkingen te melden. Bij andere middelen is er vaak onderrapportering, net omdat ze niet op zo'n grote schaal worden ingezet en minder onder de aandacht komen. Je kan het aantal meldingen over coronavaccins eigenlijk niet vergelijken met geneesmiddelen van precoronatijden."
Het FAGG publiceert maandelijks een overzicht van de bijwerkingen die zijn gemeld. Het meest recente rapport kan je hier lezen. Dat gaat voorlopig tot en met 24 januari.
Deze richtlijn is ontwikkeld voor zorgprofessionals werkzaam binnen de infectieziektebestrijding. De primaire doelgroepen zijn GGD- en LCI-professionals. De richtlijn beschrijft duidelijke adviezen, taken en verantwoordelijkheden en vormt een basis voor het nemen van geïnformeerde beslissingen en het maken van beleid in de praktijk. De zorgprofessional kan de richtlijn ook gebruiken voor het bijhouden en vergaren van kennis. De uitvoering van de richtlijn overstijgt institutionele en professionele domeingrenzen en is bedoeld voor het gebruik binnen diverse sectoren van de gezondheidszorg. Voor meer informatie zie Totstandkoming LCI-richtlijnen .
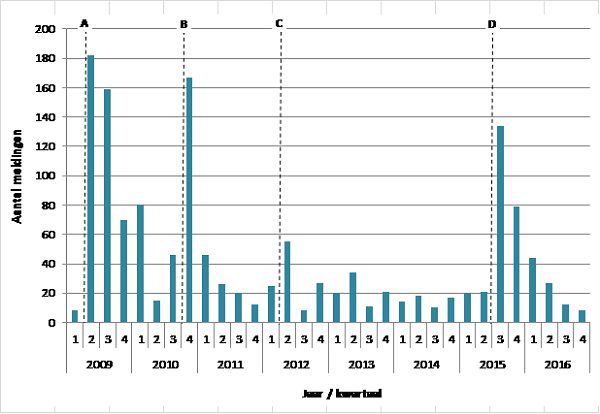
Continue surveillance van de veiligheid van vaccinaties wordt uitgevoerd door middel van een spontaan meldsysteem voor mogelijke bijwerkingen. Hiermee wordt de veiligheid van vaccins en de mogelijke bijwerkingen die na vaccinatie optreden bewaakt, waardoor tijdig actie ondernomen kan worden indien nodig. Dit spontane meldsysteem werd tot 2011 beheerd door het Rijksinstituut voor Volksgezondheid en Milieu (RIVM) en vanaf 2011 door Bijwerkingencentrum Lareb. Na deze overgang is door Lareb een campagne gestart onder ouders van gevaccineerde kinderen om melding van mogelijke bijwerkingen te promoten. Het gaat hierbij om klachten/symptomen die zijn opgetreden na vaccinatie of waarvan het vermoeden is dat het een bijwerking betreft, er hoeft dus geen sprake te zijn van een oorzakelijk verband met het vaccin. Beoordeling van meldingen vindt plaats op individuele basis, waarbij een beroep kan worden gedaan op medisch specialisten. Signalering van nieuwe (onbekende) mogelijke bijwerkingen, een nieuw aspect van een bekende bijwerking of een toename in het aantal meldingen van bepaalde klachten/symptomen die optreden na de vaccinatie vindt hierbij plaats. In het geval van een signalering wordt deze gerapporteerd aan het RIVM en het College ter Beoordeling van Geneesmiddelen ( CBG College ter Beoordeling van Geneesmiddelen (College ter Beoordeling van Geneesmiddelen) ). Het Centrum voor Infectieziektebestrijding ( CIb Centre for Infectious Disease Control (Centre for Infectious Disease Control) ) van het RIVM heeft aanvullend onderzoek uitgevoerd naar migraine en naar langdurige vermoeidheid. (14, 15)
Daarnaast is bij de introductie van HPV-vaccin (2009 en 2010) en bij de wijziging naar een 2-dosesschema (2014) in de doelgroep vragenlijstonderzoek naar de tolerabiliteit (i.e. verdraagbaarheid) uitgevoerd. (13,16-18) Dit betreft een onlinevragenlijst waarin gevraagd wordt naar het optreden van lokale en systemische klachten/symptomen in de 7 dagen na vaccinatie. In aanvulling hierop is er ten tijde van de introductie van HPV-vaccinatie (2009 en 2010) een vragenlijst tijdens de vaccinatiesessies verspreid om direct optredende klachten/symptomen te monitoren.