Winkelwagen
U heeft geen artikelen in uw winkelwagen
Diesen Eindruck hat auch Wolfgang Beyer, Mikrobiologe von der Universität Hohenheim. Er gilt als führender deutscher Phagenforscher und hat 2017 das erst deutsche Symposium zum Thema veranstaltet. In Gesprächen mit Patienten und Ärzten gewinne er oft den Eindruck, dass man den Therapieeinsatz in die "Ecke der Homöophathie schiebt". Viele glaubten, Bakteriophagen seien eine nicht ernstzunehmende, alternative Therapie. Dem sei nicht so: "Die Phagentherapie gehört ganz eindeutig zur Schulmedizin", so Beyer.
Allerdings: Klinische Studien sind rar oder ihre Qualität in der westlichen Welt umstritten. Hier gerieten die bakterienfressenden Viren ohnehin mit der Entdeckung des Penicillins Ende der 1920er-Jahre aus dem Blickfeld. In Deutschland jedenfalls ist die Phagentherapie bis heute nicht zugelassen. Und wie in vielen anderen westlichen Ländern gelten Zulassungsbestimmungen, die sich schwer tun mit Viren als Behandlungsmethode. Es gebe kein geeignetes Verfahren, sagt Bayer. In Europa gehe man davon aus, dass Medikament immer exakt reproduziert werden können. Doch genau das ist bei Phagen nicht der Fall. "Der Erfolg in Georgien beruht gerade darauf, dass sie für jede Infektion das Virus individuell anpassen können an die Infektion."
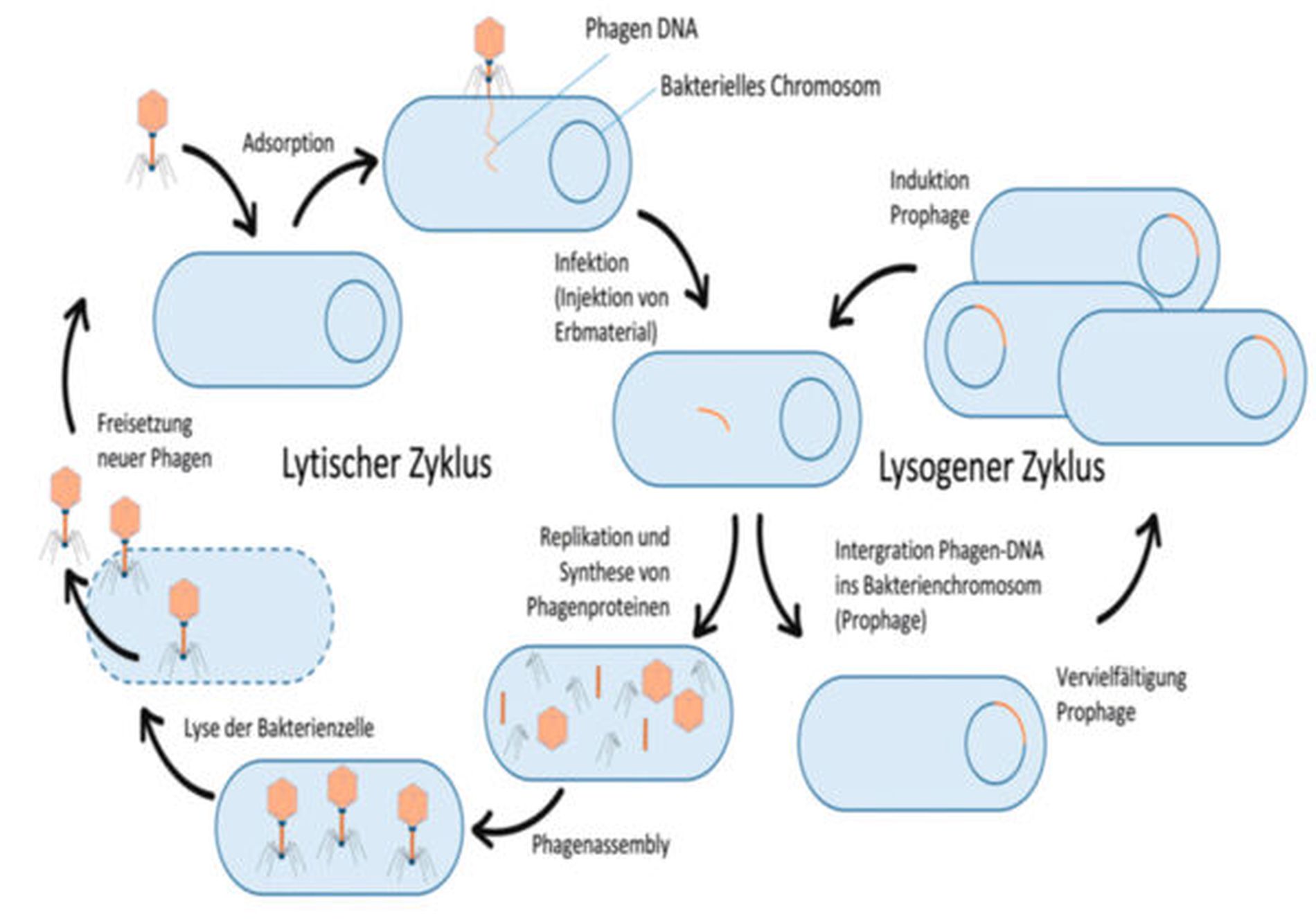
Phagen sind nicht in der Lage, sich selbst zu replizieren, sondern benötigen eine passende bakterielle Wirtszelle. Sie erkennen und binden bestimmte Strukturen auf der Oberfläche der Bakterien (Rezeptoren) und injizieren anschließend ihre genetische Information aus dem Kopf ins Zytoplasma der Bakterienzelle. Nach der Infektion nutzt der Phage die Maschinerie der Bakterienzelle zu seinen Gunsten zur Vervielfältigung des Genoms. Es werden Phagenproteine wie beispielsweise Hüllproteine und Schwänze synthetisiert, die anschließend zu intakten Phagen assemblieren. Im letzten Schritt wird die Bakterienzelle lysiert. Die neu produzierten Phagen werden in die Umgebung freigesetzt. Umliegende Bakterien können nun von den neuen Phagen infiziert werden und der Prozess beginnt von Neuem. Phagen, die sich ausschließlich auf diese Weise vermehren, folgen dem lytischen Zyklus (Abbildung 2). Beim therapeutischen Einsatz profitiert man demnach von dem natürlichen Bestreben der Phagen, sich zu vervielfältigen. Bakteriophagen sind der einzige Wirkstoff, der sich am Infektionsherd „selbstständig“ vermehrt und zwar theoretisch so lange, bis keine Wirte mehr vorhanden sind (auto-dosing effect).
Im Unterschied dazu findet bei temperenten Phagen (lysogener Zyklus) nach der Infektion ein Einbau der genetischen Information ins Genom der Bakterienzelle statt (= Prophage). Die Phagen-DNA wird mit der des Bakteriums vervielfältigt. Eine Lyse der Zelle findet nicht statt (Abbildung 2). Durch exogene Stressoren wie Antibiotika, UV-Licht, pH-Änderung, toxische Substanzen, kann es zur Freisetzung (Induktion) der Prophagen kommen. Die Phagen-DNA wird aus dem bakteriellen Genom ausgeschnitten und der lytische Zyklus weiterverfolgt. Temperente Phagen sind für die Phagentherapie aus zwei Gründen wenig geeignet. Zum einen können sie die Bakterien nicht effektiv zerstören, zum anderen besteht bei der Induktion die Gefahr, dass versehentlich unerwünschte genetische Informationen des Wirtes mit ausgeschnitten und nachfolgend auf andere Bakterien übertragen werden (Transduktion / Horizontaler Gentransfer) [Zinder, 1952].
Der Anstieg der Antibiotikaresistenzen verstärkt die Suche nach Alternativen und lässt das Interesse an Phagentherapien wieder aufleben. Phagen sind bakterienspezifische Viren und besitzen das Potenzial, gefährliche Bakterien zu zerstören. Doch bislang wurde in Europa noch kein phagenbasiertes Medikament zugelassen.
Derzeit sterben laut einer aktuellen Studie in Europa rund 30.000 Menschen jährlich an Infektionen, die durch antibiotikaresistente Bakterien verursacht werden. Werden nicht in naher Zukunft neue Therapieoptionen geschaffen, wird diese Zahl in den kommenden Jahren stark ansteigen [Cassini, 2019]. Unabhängig von der bedrohlichen Lage der Resistenzentwicklung gibt es jedoch auch Infektionen, die durch Antibiotika schwer zu behandeln sind. Sind Biofilme in die Infektion involviert, kann die Wirksamkeit von Antibiotika stark reduziert sein [Zimmerli, 2004]. Auch nimmt die Anwendung von Antibiotika einen großen Einfluss auf die Zusammensetzung des Mikrobioms, wodurch sich wiederum andere unerwünschte Bakterien etablieren können [Nylund, 2011]. Ergänzungen und Alternativen zur Behandlung von bakteriellen Infektionen werden dementsprechend dringend benötigt.
Eine neue Fallstudie aus den USA zeigt: Man kann mit Viren gegen bakterielle Infektionen vorgehen, und Antibiotikaresistenzen umgehen. Wo steht diese innovative Methode und was verspricht sie für die Zukunft? Eine Einschätzung von Wissenschaftsredaktorin Katrin Zöfel.
Klicken, um die Teilen-Funktion zu öffnen. Teilen Zu den Kommentaren springen.Katrin Zöfel ist Wissenschaftsredaktorin bei SRF. Sie ist Biologin und versucht zu verstehen, wie die Wissenschaft helfen kann, Antworten auf gesellschaftlich wichtige Fragen zu finden.
Dann beschliesst die junge Ärztin Jessica Little am Brigham and Women’s Hospital in Boston, die ihn mit behandelt: «Ich versuch’s bei ihm jetzt mit der Phagentherapie».

Vom Wahlkampf bis zur Walforschung – das Zeitfragen-Magazin von Deutschlandfunk Kultur hat den. Mehr anzeigen
"Wir sind hier, um meine Krankheit zu behandeln", sagt Detlef. Der Mittfünfziger weiß nicht mehr, wo er sich den Keim eingefangen hat. Aber er kennt den Namen: Pseudomonas aeruginosa. Ein Bakterium, das in seiner Lunge steckt. Allein in Deutschland ist der Erreger für zehn Prozent der Krankenhausinfektionen verantwortlich und damit der am häufigsten vorkommende Klinikkeim.
Seit Jahren hat Detlef, der seinen vollständigen Namen nicht nennen möchte, Beschwerden: "Ich habe nicht die Möglichkeit so durchzuatmen, wie das ein gesunder Mensch tut." Es gebe gute Tage, aber eben auch schlechte. Und desto weiter die Krankheit fortschreite in der Lunge, desto schlimmer "wird das mit der Atemnot".

Phagen sind Viren und in nahezu jedem Winkel der Erde zu finden, wodurch wir ihnen täglich ausgesetzt sind. Es gibt schätzungsweise 1031 Phagen auf der Welt [Hendrix, 2003]. Da sie wie alle Viren für die Vermehrung auf eine passende Wirtszelle angewiesen sind, sind sie vor allem dort zu finden, wo sich auch die passenden Bakterien wohlfühlen. Dabei sind sie hochspezialisiert und können meist nur einzelne Stämme innerhalb einer Bakterienspezies lysieren. Durch bestimmte Enzyme besitzen einige Phagen zudem die Fähigkeit Biofilme aufzulösen, wodurch sie Zugang zu den dort lebenden Bakterien erhalten. Besonders Abwässer, Böden und Kläranlagen, aber auch Menschen und Tiere sind reich an Mikroorganismen, so dass eine Isolation von Phagen aus Proben dieser Quellen möglich ist.
Phagen sind mit rund 50 bis 200 Nanometer um ein Vielfaches kleiner als ein Bakterium und relativ einfach aufgebaut. Die meisten bekannten Phagen gehören zur Ordnung Caudovirales und besitzen eine sogenannte Kopf-Schwanz-Struktur. Aufgrund der – elektronenmikroskopisch sichtbaren – Morphologie erfolgt die klassische Einteilung in drei Gruppen (Abbildung 1a). Die Myoviren besitzen einen kontraktilen, langen Schwanz, die Siphoviren einen nicht-kontraktilen, langen Schwanz und die Podoviren einen nicht-kontraktilen, kurzen Schwanz. Der Kopf dient zur Lagerung der DNA, während der Schwanz für die spezifische Erkennung des bakteriellen Rezeptors notwendig ist. Es gibt aber auch diverse andere Formen von Phagen, die einzelsträngige DNA oder RNA zur Speicherung der Erbinformationen nutzen. Die Größe des Genoms ist circa zehn- bis tausendfach kleiner als das von Bakterien.
Doch nicht nur im Hinblick auf ihren Aufbau sind Phagen sehr divers. Taxonomisch werden durch das International Committee on Taxonomy of Viruses (ICTV) mehr als 1.000 Spezies unterschieden [Krupovic, 2021]. Auch auf einer Agarplatte (Abbildung 1c) zeigen die Phagen in Form von Plaques („Löcher“ im Bakterienrasen) verschiedene Größen und Ausprägungen. Die Größe der Phagen, aber auch andere Wachstumsparameter, spielen bei der Plaquebildung eine Rolle. Trübe Ringe um eine klare Plaque herum – sogenannte Halos – entstehen beispielsweise, wenn Phagen Enzyme (Depolymerasen) produzieren, die die umliegenden Bakterien ebenfalls reduzieren können.